הודעת קמהדע
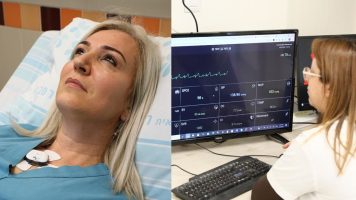
· המשתתפים במחקר הינם חולי קורונה (COVID-19) מאושפזים עם דלקת ריאות שאינם מונשמים
· במבחן ניטרול הוירוס נצפתה פעילות ניטרול מעודדת של המוצר
· פגישת Pre-IND עם מינהל התרופות והמזון האמריקני (FDA) תתקיים ברבעון הנוכחי, עם צפי להתחלת תכנית הפיתוח הקליני בארה”ב בתחילת 2021
· קמהדע מתכננת המשך בחינה של מוצר הנוגדנים כטיפול מניעתי פוטנציאלי למחלת הקורונה (COVID-19) במתנדבים בריאים המצויים בסיכון, במחקר קליני נפרד
קמהדע בע”מ , חברת ביופרמצבטיקה המתמחה במוצרים מבוססי פלסמה, מודיעה היום על גיוס החולה הראשון בישראל למחקר פאזה 1/2 במוצר הנוגדנים (IgG) מבוסס הפלסמה שפיתחה כאפשרות טיפולית למחלת הקורונה (COVID-19).
מחקר פאזה 1/2 זה, שהינו חד זרועי ויבוצע במספר מרכזים רפואיים, אושר על יד משרד הבריאות הישראלי. המחקר יבחן את הבטיחות, פארמקוקינטיקה (PK) ופארמקודינמיקה (PD) של מוצר הנוגדנים מבוסס הפלסמה בחולי COVID-19 מאושפזים עם דלקת ריאות שאינם מונשמים. 12 חולים, המתאימים לתנאי הניסוי, יגוייסו למחקר, ויטופלו במנה אחת של 4 גר’ של המוצר תוך 10 ימים מתחילת תסמיני המחלה. המעקב אחר החולים ימשך 84 ימים. במקביל, קמהדע מתכננת לבחון את מוצר הנוגדנים כטיפול מניעתי פוטנציאלי למחלת הקורנה (COVID-19), במחקר קליני נפרד, במתנדבים בריאים הנמצאים בסיכון.
יכולתו של מוצר הנוגדנים של קמהדע לנטרל את וירוס הקורונה (SARS-CoV-2) נבדקה, והתוצאות הראשוניות מעודדות ומצביעות על פוטנציאל נטרול גבוה.
“בהמשך להודעתנו ביוני האחרון כי מוצר הנוגדנים שלנו למחלת הקורונה (COVID-19) זמין לטיפול חמלה בישראל, אנו שמחים לדווח על המשך התקדמות בתכנית שלנו עם תחילתו של מחקר חשוב זה” אמר עמיר לונדון, מנכ”ל חברת קמהדע. “אנחנו מעודדים מתוצאות בדיקת ניטרול הוירוס שניצפו ומאמינים כי למוצר יש פוטנציאל להיות טיפול אפקטיבי לחולי קורונה (COVID-19) מאושפזים עם דלקת ריאות שאינם מונשמים, ואנו מצפים לתוצאות המחקר.”
אבן דרך זו הינה במסגרת הסכם שיתוף הפעולה הבין לאומי שנחתם באפריל 2020 בין קמהדע לבין חברת קדריון ביופארמה לפיתוח, יצור והפצה של נוגדן מבוסס-פלסמה (IgG) כטיפול פוטנציאלי למחלת הקורונה (COVID-19).
על מנת להרחיב את תכנית הפיתוח הקליני לארה”ב, קמהדע מתכננת, בתמיכתה של שותפתה קדריון, לקיים פגישה קדם מחקרית עבור המוצר חדש (Pre-IND) עם מינהל התרופות והמזון האמריקני (FDA) במהלך הרבעון הנוכחי, על מנת לקבל את הסכמת ה-FDA לתכנית הפיתוח הקליני המוצעת. בהתאם להסכם שיתוף הפעולה הבין-לאומי בין החברות קדריון אחראית לאיסוף פלסמת המחלימים ממחלת הקורונה (COVID-19) בארה”ב ומבצעת את האיסוף דרך חטיבת איסוף הפלסמה שלה KEDPLASMA ב-23 מרכזים מאושרי FDA ברחבי ארה”ב. אם תתקבל הסכמת ה-FDA למחקר קמהדע וקדריון מתכננות להתחיל את התכנית הקלינית בארה”ב בתחילת 2021.














השאירו תגובה
רוצה להצטרף לדיון?תרגישו חופשי לתרום!