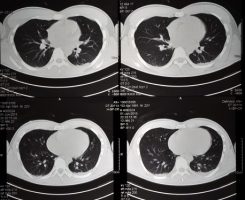
ה-FDA הודיע , וזאת כבר בפעם השנייה, על דחיית הבקשה לאשר גירסה פומית של Treprostinil (רימודולין ) לטיפול ביתר לחץ דם ריאתי (PAH). התרופה בגירסתה כזריקה (רימודולין) , וכטיפול בהשאפה (טיבסו) נמצאת כבר בשוק מס’ שנים.
בעבר דחה ה-FDA את הבקשה באוקטובר האחרון בעקבות מימצאי המחקר שערכה החברה, ה-FREEDOM-C שהראה שהמטופלים שקיבלו את הטיפול הפומי, בנוסף לטיפול בתרופות אחרות ל-PAH לא השיגו כל שיפור במרחק ההליכה ל-6 דקות בהשוואה לאלה שקיבלו פלצבו.
מאז התפרסם גם מחקר ה-FREEDOM-M , שהראה ש-151 מטופלים שאובחנו לאחרונה עם PAH וקיבלו באופן אקראי את הטיפול הפומי כטיפול יחיד הראו לאחר 12 שבועות שיפור במרחק ההליכה ל-6 דקות מאשר קבוצת בקרה שקיבלה פלצבו.
בתגובה להחלטת ה-FDA פירסמה החברה הייצרנית הודעה לפיה החברה מאמינה שלטיפול בטרפרוסטיניל פומי יש תפקיד חשוב בטיפול ב-PAH ושהחברה מחוייבת לעבוד בשיתוף פעולה עם ה-FDA בכדי להשיג את המטרה של אישור התכשיר באופן המהיר והמתאים ביותר.
















השאירו תגובה
רוצה להצטרף לדיון?תרגישו חופשי לתרום!