
הטיפ השבועי עם פרופ’ רז: השפעת אספירין על סטאטוזיס
פרופ’ רז מציג עבודה חדשה מה-JAMA שבחנה כיצד סטאוטוזיס קשורה למצבים דלקתיים, והאם אספירין יכולה לשנות את מהלך המחלה בסטאוטוזיס?

פרופ’ רז מציג עבודה חדשה מה-JAMA שבחנה כיצד סטאוטוזיס קשורה למצבים דלקתיים, והאם אספירין יכולה לשנות את מהלך המחלה בסטאוטוזיס?

מחקר שפורסם ב-The Lancet Regional Health – Americas מציע שיש להתאים את ההמלצה למרווח בין ההריונות בהתחשב בגורמים כמו היסטוריה מיילדותית אימהית

מחקר חדש שהוצג במפגש השנתי של האגודה האמריקאית לחקר הסרטן בחן האם לאימונותרפיה יש תפקיד בסביבה ניאו-אדג’ובנטית לפני ניתוח והדגים תוצאות מבטיחות
תפקידו של המיקרוביום ב-IBS מבוסס היטב, וחולים נוטלים פרוביוטיקה לעתים קרובות’ עם זאת, לא לכל הפרוביוטיקה יש יעילות שווה, אז על איזה מהם מומלץ להמליץ?

מתן טיפול ב- Vonoprazan אינו-נחות בהשוואה לטיפול תוך-ורידי במינון גבוה של מעכבי תעלות מימן במניעת דימום חוזר בתוך 30 ימים
ממאירויות משניות תועדו ב-4.3% מכלל דיווחי אירועים חריגים בקרב חולים לאחר טיפול Chimeric Antigen Recpetor T-Cell (או CAR T), כאשר

בחולים שבריריים עם אבחנה של אוטם לבבי מסוג NSTEMI (או Non-ST-Elevation Myocardial Infarction) גישה פולשנית ראשונית עשויה להיות מלווה בנזק

מנתונים חדשים שפורסמו בכתב העת Journal of the American Society of Nephrology עולה כי המטבוליט TMAO (או Trimethylamine N-Oxide) שמקורו

טיפול בגרייה מגנטית מוחית חוזרת (Repetitive Transcranial Magnetic Stimulation, או rTMS) של אזור ה-SMA (או Supplementary Motor Area) מלווה בשיפור

מנהל המזון והתרופות האמריקאי (Food and Drug Administration) העניק אישור מואץ לטיפול ב- Pontatinib לשימוש עם טיפול

מפגש יחיד של התערבות טל-רפואה המשלבת מיינדפולנס עם חמלה מפחית משמעותית תחושת דחק ותסמיני דיכאון וחרדה, כך

גירוי לשד העצם (Bone Marrow Stimulation) לא הוביל לשיפור החלמה בחולים לאחר תיקון ארתרוסקופי של מסובבי הכתף

מנתונים חדשים שהוצגו במהלך כנס ACTRIMS עולה קשר הדוק בין השמנה ובין החמרת מוגבלות, התקדמות מחלה וירידה
במאמר שפורסם בכתב העת Diabetes, Obesity & Metabolism מדווחים חוקרים על תוצאות מחקר חדש, מהן עולה כי
מנתונים חדשים שפורסמו בכתב העת JAMA Cardiology עולה כי מבחן מאמץ לב-ריאה עשוי לסייע בהערכת הדפוסים הייחודיים

בגליון זה: טכיקרדיה על-חדרית, הטיפול בחסר ויטמין D בילדים, בקיצור נמרץ ועוד

חסר בויטמין D נפוץ מאוד בילדים ובמתבגרים באופן גלובלי. בגיל הילדות חסר זה יכול להוביל לרככת, לנכות ואף לתחלואה מסכנת חיים. בעשור השני לחיים מסת העצם גדלה משמעותית ולכן גיל ההתבגרות הינו תקופה קריטית לבריאות העצם בהמשך החיים. מעבר לכך, הידע לגבי השפעותיו הגופניות של ויטמין D שאינן קשורות בבריאות העצם הולך ומתרחב. קיימת חשיבות רבה להקפדה על ערכי ויטמין D תקינים בגיל הילדות וההתבגרות. מוצגות כאן יחד עמדת המומחים באנדוקרינולוגיה מהעיתון expert opinion of endocrinology and metabolism ונייר העמדה של האיגוד לרפואת המתבגרים, שפורסם בעיתון לרפואת המתבגרים, כדי לסכם את ההמלצות הנוגעות לבירור ולטיפול בחסר בויטמין D בילדים ובמתבגרים.

במאמר שפורסם בכתב העת JAMA מדווחים חוקרים על תוצאות מחקר חדש, מהן עולה כי בפגים עם בקע מפשעתי, השלמת תיקון בקרע לאחר השחרור מיחידת טיפול נמרץ ביילודים הובילה לשיעור נמוך יותר של אירועים חריגים, בהשוואה לפרוצדורות שבוצעו לפני השחרור מבית החולים. ד”ר ברזילי, עורך מדור נאונטולוגיה מוסיף מהערותיו.

מטה אנליזה וסקירה סיסטמתית (מחקר משולב) שפורסמה לאחרונה ב-JAMA PEDIATRICS, עסקה בבריאותם הנפשית של ילדים ובני נוער עם פגיעה נוירולוגית-התפתחותית, על מנת לבחון את הקשר בין פעילות גופנית לפרמטרים של בריאות נפשית: תפקוד קוגניטיבי, בריאות נפשית-פסיכולוגית, הכללת והפנמת בעיות. ד”ר עדי זיו, עורך מדור ילדים, משתף את המאמר ומוסיף מהערותיו.

גולש יקר ! ידיעה זו מיועדת לסגל הרפואי בלבד ואינה מאושרת לצפייה לקהל הרחב. אנא בצע LOG

גולש יקר ! ידיעה זו מיועדת לסגל הרפואי בלבד ואינה מאושרת לצפייה לקהל הרחב. אנא בצע LOG

במגזין הנוכחי: הטיפול בחסר ויטמין D בילדים, מאפייני תיאבון והתפתחות הפרעות אכילה, בקיצור נמרץ – ועוד

חסר בויטמין D נפוץ מאוד בילדים ובמתבגרים באופן גלובלי. בגיל הילדות חסר זה יכול להוביל לרככת, לנכות ואף לתחלואה מסכנת חיים. בעשור השני לחיים מסת העצם גדלה משמעותית ולכן גיל ההתבגרות הינו תקופה קריטית לבריאות העצם בהמשך החיים. מעבר לכך, הידע לגבי השפעותיו הגופניות של ויטמין D שאינן קשורות בבריאות העצם הולך ומתרחב. קיימת חשיבות רבה להקפדה על ערכי ויטמין D תקינים בגיל הילדות וההתבגרות. מוצגות כאן יחד עמדת המומחים באנדוקרינולוגיה מהעיתון expert opinion of endocrinology and metabolism ונייר העמדה של האיגוד לרפואת המתבגרים, שפורסם בעיתון לרפואת המתבגרים, כדי לסכם את ההמלצות הנוגעות לבירור ולטיפול בחסר בויטמין D בילדים ובמתבגרים.

להרצאה לחצו כאן

לפניכם הרצאות הוובינר שהתקיים ב-13.3.24 בהשתתפות ד”ר עידית דותן, ד”ר טלי שטיינמץ וד”ר קרן סקלסקי. להרצאות לחצו כאן
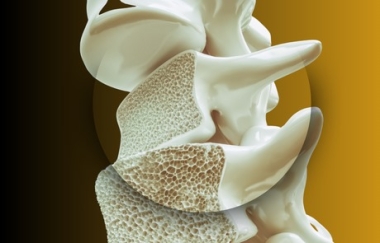
לפניכם הקלטת המפגש בהנחיית ד”ר פנינה רוטמן-פיקלני ובהשתתפות פרופ’ דויד קנדלר. לאחר הרצאתו של פרופ’ דויד קנדלר
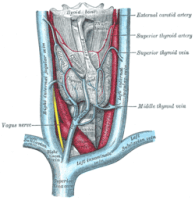
לפניכם הקלטת המפגש שהתקיים ב-4.3.24, בהנחיית ד”ר נטלי לרנר מהאיגוד הישראלי לרפואת המשפחה ובהשתתפות פרופ’ איל רובינשטוק,

לפניכם הקלטת המפגש שהתקיים ב-26.2.24, בהנחיית ד”ר נטלי לרנר מהאיגוד הישראלי לרפואת המשפחה ובהשתתפות ד”ר נירית לב,

לפניכם הרצאה ודיון בין ד”ר ליאת ברזילי יוסף ופרופ’ איתמר רז על איזון חשיבות האיזון הגליקמי, מתוך

לפניכם הרצאות הוובינר שהתקיים ב7.3.24 מטעם המועצה הלאומית לסוכרת ובהנחיית ד”ר יואל טולדנו. דברי פתיחה ומבוא, ד”ר

לפניכם הרצאות הוובינר שהתקיים ב21.2.24 ביוזמת ספרת הסוכרת בגליל. פרופ’ נעים שחאדה וד”ר ריאד טאהר נותנים סקירה

בשנה ה-22 ברציפות: כנס Biomed Israel 2024 ייערך בסוף מאי בתל אביב ויציג את מיטב החידושים של תעשיית מדעי החיים הישראלית; למעלה מ-100 חברות יציגו את הפתרונות והטכנולוגיות שפיתחו ויספקו הזדמנות ייחודית לאלפי המבקרים להתעדכן בחדשנות בתחומי הביומד וטכנולוגיות הבריאות

סקר חדש ומקיף שערכה מכבי שירותי בריאות במלאת חצי שנה למלחמת ‘חרבות ברזל’ חושף את המצב הבריאותי של הציבור הישראלי, כפי שהוא עצמו תופס אותו, רגע לפני חג הפסח. מהסקר עולה נתון מדאיג: עליה של יותר מ-100% בשיעור האזרחים שתופסים את מצבם הבריאותי כבינוני או גרוע בהשוואה לתקופה שלפני המלחמה

בהודעה משותפת למשרד האוצר ומשרד הבריאות, מנכ”לי המשרדים קבעו היום כי ההקמה והתפעול של בית החולים החדש בבאר שבע יהיה במודל משולב של קופות החולים מאוחדת ולאומית ובית החולים שיבא, תוך שהבעלות תהיה של קופות החולים וההפעלה תהיה על ידי בית החולים שיבא שעימו יתקשרו הקופות.

ד”ר זאהר חורי מונה למנהל מחלקה פנימית א’ במרכז רפואי צפון (פוריה). ד”ר זאהר חורי, מומחה למחלות ריאה ורפואה פנימית הגיע למרכז הרפואי צפון מבי”ח העמק

במסגרת מחקר בין-לאומי משותף, שלושה מדענים מהטכניון ועמיתיהם בגרמניה יחקרו את המנגנונים המולקולארים המייצבים אונקו-פרוטאינים בסרטן.

הכנס השנתי הגדול בישראל למטפלים ברפואה משלימה ואינטגרטיבית יתקיים בתאריכים 5-6.7.20225 עד 6 ביולי 2022! מפגש פסגה של 1,500 מטפלים

כיצד יראה עולם הרפואה בעוד 20 שנה? על השאלות האלו יענו גדולי המומחים מישראל ומהעולם בכנס החשוב והמוביל ביותר בעולם

ביום שני הקרוב 16.5.22 יתקיים הכנס השנתי של בריאות הציבור במכללה האקדמית אשקלון בשיתוף הגופים המובילים את

האירוע השנתי של תעשיית מדעי החיים בישראל; בין הדוברים: מייקל דולסטן פייזר, פרופ’ רוברט לנגר ועוד. זו השנה
המפגש יתקיים בזום, ב 12 במאי 2022, בין השעות 09:00 15:00. להרשמה לחצו כאן לתוכנית לחצו כאן
נא ציין כתובת דואר אלקטרוני שבה אתה מקבל דיוורי e-Med או זו שציינת בכרטיס האישי שלך.
קישור לאיפוס סיסמא נשלח למייל.
חזרה להתחברות
תגובות אחרונות