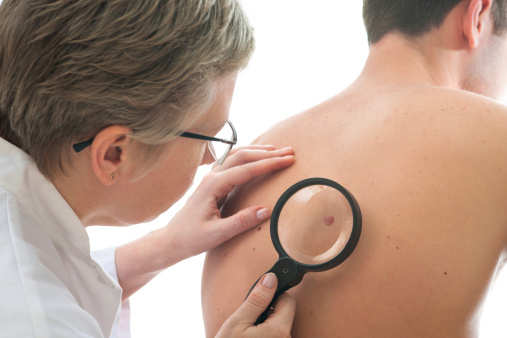
גיל מבוגר ומין זכר מלווים בסיכון מוגבר לאבחנה של מלנומה ראשונית נוספת (JAMA Dermatol)
לאחר אבחנה ראשונה של מלנומה פולשנית ראשונית, גיל מבוגר ומגדר זכרי הינם גורמי סיכון אפשריים לאבחנה של מלנומה נוספת בשלב

לאחר אבחנה ראשונה של מלנומה פולשנית ראשונית, גיל מבוגר ומגדר זכרי הינם גורמי סיכון אפשריים לאבחנה של מלנומה נוספת בשלב

אימון שרירי רצפת אגן מלווה בשיפור בתפקוד המיני בנשים עם הפרעה בתפקוד רצפת האגן, כולל שיפור עוררות מינית, אורגזמה, שביעות

במאמר שפורסם בכתב העת International Journal of Cancer מדווחים חוקרים על תוצאות מחקר חדש, מהן עולה כי שתיית קפה עשויה

איזוטרטינואין (רואקוטן) הינה נגזרת של רטינואידים (ויטמין A) המשמשת לטיפול באקנה וולגריס (Acne Vulgaris) קשה שלא הגיבה לקוי טיפול מוקדמים. ד”ר עדי זיו, עורך מדור ילדים, משתף מחקר מה-JAMA Dermatology שעסק בהערכת הסיכון היחסי והמוחלט לאובדנות ולתחלואה נפשית בקרב המשתמשים באיזוטרטינואין, ומוסיף מהערותיו.

פרופ’ רז עוסק בהפסקת/לקיחת אספירין במטופלים, ומתייחס למאמר שפורסם לאחרונה ב-JAMA בו נמצא שבמטופלים ללא אינדיקציה לנטילת אספירין, הפסקת הטיפול
עדויות חדשות תומכות בבטיחות טיפול חליפי בטסטוסטרון בגברים בגיל העמידה וגברים מבוגרים יותר עם היפוגונאדיזם, כאשר אין עדות לעליה בסיכון

מחקר פאזה 2 ב-sonelokimab במתן תת עורי הדגים תגובה קלינית משמעותית בחולי הידרדניטיס סופורטיביה, כך עולה מניסוי קליני אקראי שהוצג במפגש השנתי של האקדמיה האמריקאית לרפואת עור
בחולים עם רמות גבוהות של טריגליצרידים הנמצאים בסיכון לדלקת לבלב, התרופה הניסיונית plozasiran הביאה להפחתה ברמות הטריגליצרידים, כך עולה ממחקר שפורסם ב-JAMA Cardiology

ההנחיות הקליניות הראשונות בארה”ב לאבחון ולטיפול בהפרעות קשב וריכוז (ADHD) אצל מבוגרים צפויות להתפרסם בסתיו הקרוב, ולספק לחולים, רופאים, וקובעי מדיניות מסגרת סטנדרטית שהייתה נחוצה מזה זמן רב
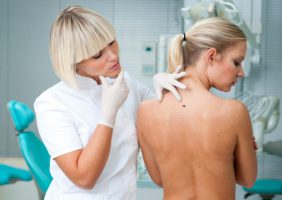
מנתונים חדשים שפורסמו בכתב העת Journal of Investigative Dermatology עולה כי מתן Rilzabrutinib בשילוב עם סטרואידים במינון

מנתונים חדשים שפורסמו בכתב העת Clinical Gastroenterology and Hepatology עולה כי Upadacitinib (רינבוק) הוביל לשיפור תדירות צואה
מנתונים חדשים שפורסמו בכתב העת Diabetes Care עולה כי טיפול ב- Tirzepatide(מאונג’רו) הוביל לשיפור גדול יותר מאינסולין
מתן מעכבי תעלות מימן פעמיים ביום מלווה בשיעורי תגובה היסטולוגית גבוהים יותר בחולים עם דלקת וושט אאזנופילית

מנהל המזון והתרופות האמריקאי (Food and Drug Administration) הודיע על החלטה סופית להסרת אישור הטיפול ב-Melphalan (מלפלן)

למרות חשש מפני תביעות רשלנות רפואית של רופאים, חוקרים לא מצאו עליה בתביעות רשלנות רפואית מוצלחות על-רקע

במאמר שפורסם בכתב העת New England Journal of Medicine מדווחים חוקרים על תוצאות מחקר חדש בו הגיוס למחקר בשלב מוקדם בשל סוגיות הנוגעות לבטיחות ההתערבות, כאשר חיסון אימהי כנגד RSV המבוסס על Perfusion F Protein אמנם הפחית סיכון לסיבוכים משנית למחלה בדרכי נשימה תחתונות על-רקע RSV, אך לווה בעליה בסיכון ללידה מוקדמת. ד”ר ברנרד ברזילי, עורך מדור ניאונטולוגיה, משתף את המאמר ומוסיף מהערותיו

איזוטרטינואין (רואקוטן) הינה נגזרת של רטינואידים (ויטמין A) המשמשת לטיפול באקנה וולגריס (Acne Vulgaris) קשה שלא הגיבה לקוי טיפול מוקדמים. ד”ר עדי זיו, עורך מדור ילדים, משתף מחקר מה-JAMA Dermatology שעסק בהערכת הסיכון היחסי והמוחלט לאובדנות ולתחלואה נפשית בקרב המשתמשים באיזוטרטינואין, ומוסיף מהערותיו.

חסר בויטמין D נפוץ מאוד בילדים ובמתבגרים באופן גלובלי. בגיל הילדות חסר זה יכול להוביל לרככת, לנכות ואף לתחלואה מסכנת חיים. בעשור השני לחיים מסת העצם גדלה משמעותית ולכן גיל ההתבגרות הינו תקופה קריטית לבריאות העצם בהמשך החיים. מעבר לכך, הידע לגבי השפעותיו הגופניות של ויטמין D שאינן קשורות בבריאות העצם הולך ומתרחב. קיימת חשיבות רבה להקפדה על ערכי ויטמין D תקינים בגיל הילדות וההתבגרות. מוצגות כאן יחד עמדת המומחים באנדוקרינולוגיה מהעיתון expert opinion of endocrinology and metabolism ונייר העמדה של האיגוד לרפואת המתבגרים, שפורסם בעיתון לרפואת המתבגרים, כדי לסכם את ההמלצות הנוגעות לבירור ולטיפול בחסר בויטמין D בילדים ובמתבגרים.

המועצה הלאומית לסוכרת והחברה הישראלית לחקר ולטיפול בהשמנה: זמינות וויגובי לטיפול בהשמנה בישראל מהווה הזדמנות המלווה בהתחייבות גדולה של ציבור הרופאים לאפשר מתן טיפול אחראי, יעיל, מוסדר ורציף הן בחולים החיים עם השמנה ובמצבים מסוימים גם במטופלים הסובלים מסוכרת והשמנה, שלא הגיעו למשקל הרצוי. לאור זאת, המועצה הלאומית לסוכרת יחד עם החברה הישראלית לחקר וטיפול בהשמנה, ניסחו קווים מנחים לטיפול בוויגובי.

עצירות אידיופתית כרונית היא בעיה בריאותית נפוצה, המשפיעה באופן משמעותי על איכות החיים של אלה הסובלים מכך. הפרעה זו מחייבת גישה רב-תחומית לטיפול, המשלבת התאמות תזונתיות ושימוש בטיפולים, הן בלא מרשם, הן בתרופות מרשם, לניהול יעיל של התסמינים. בהקשר זה, רוקחים מתגלים כאנשי מקצוע חיוניים בתחום הבריאות, ומציעים הדרכה חיונית לחולים בהתבסס על ההמלצות המפורטות בהנחיות הקליניות של האגודה האמריקנית לגסטרואנטרולוגיה לשנת 2023 – המכללה האמריקנית לגסטרואנטרולוגיה (AGA/ACG): ניהול פרמקולוגי של עצירות אידיופתית כרונית.

מחקר זה מתעמק באתגרים העומדים לפני צעירים הסובלים מאסתמה, תוך דגש על ההיענות לקורטיקוסטרואידים בשאיפה (ICS), טיפול מרכזי באסתמה מתמשכת.

גולש יקר ! ידיעה זו מיועדת לסגל הרפואי בלבד ואינה מאושרת לצפייה לקהל הרחב. אנא בצע LOG

גולש יקר ! ידיעה זו מיועדת לסגל הרפואי בלבד ואינה מאושרת לצפייה לקהל הרחב. אנא בצע LOG

לפניכם הרצאות הוובינר שהתקיים ב-13.3.24 בהשתתפות ד”ר עידית דותן, ד”ר טלי שטיינמץ וד”ר קרן סקלסקי. להרצאות לחצו כאן
לפניכם הקלטת המפגש בהנחיית ד”ר פנינה רוטמן-פיקלני ובהשתתפות פרופ’ דויד קנדלר. לאחר הרצאתו של פרופ’ דויד קנדלר הועלו מספר מקרים

לפניכם הרצאה ודיון בין ד”ר ליאת ברזילי יוסף ופרופ’ איתמר רז על איזון חשיבות האיזון הגליקמי, מתוך

לפניכם הרצאות הוובינר שהתקיים ב7.3.24 מטעם המועצה הלאומית לסוכרת ובהנחיית ד”ר יואל טולדנו. דברי פתיחה ומבוא, ד”ר

לפניכם הרצאות הוובינר שהתקיים ב-5.2.24 בהנחיית ד”ר ריאד טאהר ובהשתתפות ד”ר שולי הית’אם ופרופ’ ארמלי זאהר.

לפניכם פודקאסט עם ד”ר יפעת ויגיסר, היחידה הנוירואימונולוגית, מרכז רפואי תל-אביב, בנושא הגישות האסטרטגיות השונות לטיפול בטרשת

לפניכם פודקאסט עם ד”ר קרן רגב, מנהלת שירות טרשת נפוצה, מרכז רפואי תל-אביב, בנושא תכנון משפחה עם

לפניכם פודקאסט עם ד”ר שי מנשקו, המרכז לטרשת נפוצה, בית החולים השיקומי, המרכז הרפואי ע”ש שיבא תל

מנהל בית החולים ‘אסותא’ אשדוד, ד”ר ארז ברנבוים, מנהל המרכז הרפואי האוניברסיטאי ברזילי, ד”ר חזי לוי, ומנהל המרכז הרפואי האוניברסיטאי סורוקה, ד”ר שלומי קודש יקבלו השנה את ‘פרס נשיא האוניברסיטה’ במסגרת חבר הנאמנים של אוניברסיטת בן-גוריון בנגב.

המוקד, המופעל ממטעם ארגון הרוקחות בישראל בשיתוף האגודה לזכויות החולה בישראל ייפתח מחדש השבוע במתכונתו המחודשת. המוקד יתן מענה מקצועי לא רק לשאלות מצד הקהל הרחב, אלא גם לשאלות קליניות מצד צוותי הרפואה והפרא-רפואה. מספר טלפון מוקד הייעוץ הרוקחי-קליני מטעם ארגון הרוקחות בישראל כוכבית 9711 *. המוקד פעיל בימים א’, ג’, ה’ בין השעות 10:00 – 13:00, ובימים ב’ ו-ד’ בין השעות 16:00 – 19:00. המוקד זמין בשפות עברית, אנגלית, ערבית ורוסית.

יו”ר ארגון הרוקחות בישראל, פרופ’ איל שורצברג, נבחר מחדש כיו”ר הארגון לקדנציה נוספת, השנייה שלו כיו”ר הארגון.

לקראת חג הפסח משרד הבריאות בשיתוף המרכז הארצי למידע בהרעלות במרכז רפואי ברמב”ם וארגון בטרם לבטיחות ילדים, מפרסמים נתונים על הרעלות בעקבות חומרי ניקיון וכללים לבטיחות השימוש בחומרי ניקיון בבית.

מנתוני משרד הבריאות שפורסמו בדו”ח כוח האדם לשנת 2022 שיצא לאור לאחרונה, עולה כי 63% מקהל הרוקחים בישראל הם נשים. על פי הנכתב בדו”ח, אחוז זה שומר על יציבות במהלך העשור האחרון.

הכנס השנתי הגדול בישראל למטפלים ברפואה משלימה ואינטגרטיבית יתקיים בתאריכים 5-6.7.20225 עד 6 ביולי 2022! מפגש פסגה של 1,500 מטפלים

מצב דרך ההרשמה לקורסים החדשים הנפתחים בחודשים הקרובים: לאתר המדור לחצו כאן בבקשה לקישור ישיר להרשמה, לחצו כאן בבקשה

האיגוד הנוירולוגי בשילוב העמותה הישראלית למדעי המוח ועמותות החולים מזמינים את הקבל הרחבליריד המוח-נפלאות המוח בבריאות ובחולי.

פרטים נוספים והרשמה באתר המדור: לחצו כאן בבקשה לברושור כללי קורס קנביס לסילבוס רישום ורגולציה לסילבוס מרשם

בסוף השבוע (25-27 באוקטובר) מתקיים הכנס הארצי לפרמקולוגיה מודרנית של המרכז הרפואי זיו בצפת, בשיתוף פורום מנהלי
נא ציין כתובת דואר אלקטרוני שבה אתה מקבל דיוורי e-Med או זו שציינת בכרטיס האישי שלך.
קישור לאיפוס סיסמא נשלח למייל.
חזרה להתחברות
תגובות אחרונות