מנהל המזון והתרופות האמריקאי (Food and Drug Administration) קיבל בקשה לאישור Roflumilast, מעכב מקומי של PDE4 (Phosphodiesterase Type 4) לטיפול בפסוריאזיס במבגרים ובמתבגרים, כך על-פי הצהרה מטעם היצרן.
קרם Roflumilast הוא מעכב של PDE4 אנזים המעלה מדדים פרו-דלקתיים ומפחית מדדים נוגדי-דלקת. המומחים מסבירים כי PDE4 הוא יעד טיפול מוכח ברפואת עור: מנהל המזון והתרופות האמריקאי אישר את מעכב PDE4, Crisaborole כטיפול מקומי לאטופיק דרמטיטיס בדרגה קלה-עד-בינונית בשנת 2016 ובוחן את אישור טיפול פומי במעכב PDE-4, Orismilast, לטיפול בפסוריאזיס רובדית.
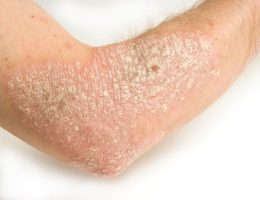
טיפול מקומי ב- Roflumilast, במידה ויאושר, צפוי להיות התכשיר הראשון ממשפחת מעכבי PDE4 המיועד לטיפול בפסוריאזיס. הקרם נועד לשמש בכל הגוף, כולל הפנים ואזורים רגישים בין הקפלים.
הבקשה לאישור הטיפול מבוססת על נתונים מזוג מחקרים אקראיים,, כפלי-סמיות, בשלב 3, המוכרים בשם DERMIS 1 ו-DERMIS 2, אשר בחנו את השימוש ב- Roflumilast לטיפול בפסוריאזיס רובדית ושלב ארוך-טווח בתווית-פתוחה.
מחקרי DERMIS 1 ו-DERMIS 2 היו מחקרים רב-מרכזיים, בינלאומיים, זהים, אשר נועדו לבחון את הבטיחות והיעילות של קרם Roflumilast 0.3%. במחקרים אלו, Roflumilast ענה על התוצא העיקרי ובחולים שטופלו בתכשיר תועדו שיעורי הצלחה של 42.4%, בהשוואה ל-6.1% בזרוע הפלסבו (p<0.0001) ושל 37.5% לעומת 6.9%, בהתאמה, במחקרי DERMIS 1 ו-DERMIS 2.
במחקר בשלב 2b, ההשפעה של הטיפול נותרה למשך 52-64 שבועות. הטיפול ב- Roflumilast נסבל היטב בשלושת המחקרים.
בסיכומו של דבר, האירועים החריגים הנפוצים ביותר עליהם דווח במחקרים כללו שלשול (3%), כאבי ראש (2%), נדודי שינה (1%), בחילות (1%), זיהומים בדרכי נשימה עליונות (1%) וזיהומים בדרכי נשימה תחתונות (1%).
הטיפול ב- Roflumilast גם הדגים שיפור מובהק סטטיסטית לעומת פלסבו בתוצאי סיום משניים, כולל מדדי Intertriginous Investigator Global Assessment, מדד Psoriasis Area Severity Index-75, הקלה בגרד והערכת התסמינים בעיניי החולים.
מתוך הודעת ה-FDA












השאירו תגובה
רוצה להצטרף לדיון?תרגישו חופשי לתרום!