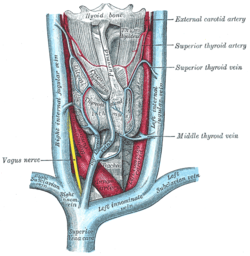
השוואת ההשפעה של גישות טיפול שונות לפעילות יתר של בלוטת התריס על הסיכון הלבבי (JAMA Netw Open)
ניתוח וטיפול ביוד רדיואקטיבי מלווים בסיכון מופחת לסיבוכים קרדיווסקולאריים מג’וריים בטווח הארוך, בהשוואה לטיפול ארוך טווח בתרופות כנגד בלוטת התריס

ניתוח וטיפול ביוד רדיואקטיבי מלווים בסיכון מופחת לסיבוכים קרדיווסקולאריים מג’וריים בטווח הארוך, בהשוואה לטיפול ארוך טווח בתרופות כנגד בלוטת התריס

תרופות ממשפחת מעכבי SGLT-2 (או Sodium Glucose Cotransporter) עשויות לסייע בהפחתת הסיכון לאנמיה בחולים עם סוכרת מסוג 2 ומחלת כליות

סוכר טבעי (D-Mannose) המשמש לטיפול בזיהומים חוזרים בדרכי השתן לא הפחית את הסיכון לאירועים חוזרים, ביקורים אמבולטוריים, טיפול אנטיביוטי, או

האם התיעוד המפרך של ראומטולוגים את פעילות המחלה ואת התוצאות המדווחות על ידי המטופלים במשך עשרות שנים, יכול לסייע לבינה המלאכותית לחזות תוצאות של מטופלים?

פרופ’ רז מציג עבודה חדשה מה-JAMA שבחנה כיצד סטאוטוזיס קשורה למצבים דלקתיים, והאם אספירין יכולה לשנות את מהלך המחלה בסטאוטוזיס?

מחקר שפורסם ב-The Lancet Regional Health – Americas מציע שיש להתאים את ההמלצה למרווח בין ההריונות בהתחשב בגורמים כמו היסטוריה מיילדותית אימהית

מתן טיפול ב- Vonoprazan אינו-נחות בהשוואה לטיפול תוך-ורידי במינון גבוה של מעכבי תעלות מימן במניעת דימום חוזר בתוך 30 ימים

בחולים שבריריים עם אבחנה של אוטם לבבי מסוג NSTEMI (או Non-ST-Elevation Myocardial Infarction) גישה פולשנית ראשונית עשויה להיות מלווה בנזק

זירת טרור נרחבת ובה 1,200 נרצחים ויותר מ-9,000 פצועים הינה אירוע בסדר גודל מגה המוני. בדו”ח משותף לאוניברסיטת בן-גוריון בנגב ומד”א, מפורטים רצף ושפע האירועים הרפואיים, החל מהשעה 6:30 בבוקר שבת של ה-7/10 ועד סוף אותו היום. דו”ח זה מציף את האתגרים עימם התמודדו צוותי הרפואה האזרחיים בשטח וממצאיו פורסמו בכתב העת International Journal of Public Health

מאז תחילת המלחמה, פונו לבתי החולים ;15,333 פצועים, בקליטה סטטוס הפציעה שלהם היה 693 במצב קשה או אנוש, 1,287 במצב בינוני, 689 נפגעי חרדה ונפש ו-12,318 במצב קל. משרד הבריאות מעדכן על 151 פצועים המאושפזים בבתי החולים כעת (נכון ל-18/4/24).

מחקר חדש מראה תוצאות תפקודיות משופרות לפינוי קריש כירורגית בתוספת ניהול רפואי, כך עולה מניסוי ה-ENRICH שפורסם ב-The New England Journal of Medicine

למרות חשש מפני תביעות רשלנות רפואית של רופאים, חוקרים לא מצאו עליה בתביעות רשלנות רפואית מוצלחות על-רקע
במאמר שפורסם בכתב העת Journal of the American College of Cardiology מדווחים חוקרים על תוצאות מחקר חדש,

במאמר שפורסם בכתב העת International Journal of Cardiology מדווחים חוקרים על תוצאות מחקר חדש, מהן עולה כי
במאמר שפורסם בכתב העת Cureus מדווחים חוקרים על תוצאות מחקר חדש, מהן עולה כי רמות CRP (או

בגליון זה: טכיקרדיה על-חדרית, הטיפול בחסר ויטמין D בילדים, בקיצור נמרץ ועוד

חסר בויטמין D נפוץ מאוד בילדים ובמתבגרים באופן גלובלי. בגיל הילדות חסר זה יכול להוביל לרככת, לנכות ואף לתחלואה מסכנת חיים. בעשור השני לחיים מסת העצם גדלה משמעותית ולכן גיל ההתבגרות הינו תקופה קריטית לבריאות העצם בהמשך החיים. מעבר לכך, הידע לגבי השפעותיו הגופניות של ויטמין D שאינן קשורות בבריאות העצם הולך ומתרחב. קיימת חשיבות רבה להקפדה על ערכי ויטמין D תקינים בגיל הילדות וההתבגרות. מוצגות כאן יחד עמדת המומחים באנדוקרינולוגיה מהעיתון expert opinion of endocrinology and metabolism ונייר העמדה של האיגוד לרפואת המתבגרים, שפורסם בעיתון לרפואת המתבגרים, כדי לסכם את ההמלצות הנוגעות לבירור ולטיפול בחסר בויטמין D בילדים ובמתבגרים.

בקיצור נמרץ – לקט מחקרים מן המחצית השניה של חודש מארס 2024

במגזין זה: קוצבי לב ודפיברילטורים מושתלים, ניוון מקולרי גילי, בקיצור נמרץ ועוד

גולש יקר ! ידיעה זו מיועדת לסגל הרפואי בלבד ואינה מאושרת לצפייה לקהל הרחב. אנא בצע LOG

לקט מחקרים מן המחצית הראשונה של חודש פברואר 2024

במגזין הפעם – אלרגיות למזון ואנפילקסיס הקשור למזון, סיפור מקרה על קוצר נשימה מתקדם במאמץ, בקיצור נמרץ עוד

גולש יקר ! ידיעה זו מיועדת לסגל הרפואי בלבד ואינה מאושרת לצפייה לקהל הרחב. אנא בצע LOG

ב-1 בנובמבר התקיים וובינר שעסק בניהול טראומה ראשונית ונפשית, במסגרת מיזם “איגודים נפגשים” של האיגוד הישראלי לרפואת המשפחה, שאירח את

לפניכם ההרצאה והדיון שנערך בעקבותיה עם ד”ר טוביה בן גל, מנהל היחידה לאי ספיקת לב, מרכז רפואי רבין וד”ר דבי

לפניכם הרצאות קצרות על עדכונים באימונותרפיה לטיפול בסרטן עם פרופ’ גל מרקל. בחסות בלתי תלויה של

לפניכם הרצאה ודיון שנערכו במסגרת קצר קולע וממוקד – סוגיות בתוספי תזונה ההרצאה בחסות חברת אלטמן

הכנסו לאתר האקדמיה לנאונטולוגיה לצפייה בהקלטת הוובינר הבינלאומי שהתקיים ב-7.6.2021 בהנחיית ד”ר ברנרד ברזילי
אם אינך רואה מייל זה תקין לחצ/י כאן מהתיאוריה לפרקטיקה במחלקה הפנימית בטיפול בנוזלי עירוי פרופ’ אבישי
אי ספיקת לב – סיקור מפגש ראשון מה-26.5.2021 במפגש ראשון זה הוצגו הגישות לאבחנה וטיפול באי ספיקת

מרשם להחייאת נוזלים: לקבוע מבלי לטבוע פרופ’ אבישי אליס וד”ר שאול לב בחלק הראשון הציג ד”ר שאול

מינוי חדש במרכז רפואי צפון: ד”ר מערוף מוסא מונה למנהל המלר”ד (המחלקה לרפואה דחופה) – המיון במרכז רפואי צפון (פוריה). מנהל המחלקה לרפואה דחופה (המלר”ד), ד”ר מערוף מוסא הגיע מהמרכז הרפואי בני ציון בחיפה

סקר חדש ומקיף שערכה מכבי שירותי בריאות במלאת חצי שנה למלחמת ‘חרבות ברזל’ חושף את המצב הבריאותי של הציבור הישראלי, כפי שהוא עצמו תופס אותו, רגע לפני חג הפסח. מהסקר עולה נתון מדאיג: עליה של יותר מ-100% בשיעור האזרחים שתופסים את מצבם הבריאותי כבינוני או גרוע בהשוואה לתקופה שלפני המלחמה

בהודעה משותפת למשרד האוצר ומשרד הבריאות, מנכ”לי המשרדים קבעו היום כי ההקמה והתפעול של בית החולים החדש בבאר שבע יהיה במודל משולב של קופות החולים מאוחדת ולאומית ובית החולים שיבא, תוך שהבעלות תהיה של קופות החולים וההפעלה תהיה על ידי בית החולים שיבא שעימו יתקשרו הקופות.

מנהל בית החולים ‘אסותא’ אשדוד, ד”ר ארז ברנבוים, מנהל המרכז הרפואי האוניברסיטאי ברזילי, ד”ר חזי לוי, ומנהל המרכז הרפואי האוניברסיטאי סורוקה, ד”ר שלומי קודש יקבלו השנה את ‘פרס נשיא האוניברסיטה’ במסגרת חבר הנאמנים של אוניברסיטת בן-גוריון בנגב.

המוקד, המופעל ממטעם ארגון הרוקחות בישראל בשיתוף האגודה לזכויות החולה בישראל ייפתח מחדש השבוע במתכונתו המחודשת. המוקד יתן מענה מקצועי לא רק לשאלות מצד הקהל הרחב, אלא גם לשאלות קליניות מצד צוותי הרפואה והפרא-רפואה. מספר טלפון מוקד הייעוץ הרוקחי-קליני מטעם ארגון הרוקחות בישראל כוכבית 9711 *. המוקד פעיל בימים א’, ג’, ה’ בין השעות 10:00 – 13:00, ובימים ב’ ו-ד’ בין השעות 16:00 – 19:00. המוקד זמין בשפות עברית, אנגלית, ערבית ורוסית.
שלום לכולם, האקדמיה לניאונטולוגיה אירגנה וובינר בינלאומי בנושא ניהול נוזלים ופרמקולוגיה בניאונטולוגיה. הוובינר ייערךביום ה’ 25.3.21 בשעה 18:00 שעון ישראל.

לצפייה בהזמנה ובתכנית המפגש הקליקו כאן להרשמה הקליקו כאן

מצורפת הזמנה וקישור לרישום לוובינר. שימו לב שישלהרשם מראש

מצורפת הזמנה וקישור לרישום לוובינר. שימו לב שישלהרשם מראש
שלום רב, בשעה טובה ומוצלחת אני שולח לכם את תכנית כנס האקדמיה לניאונטולוגיה 2019. השנה הכנס יתמקד
נא ציין כתובת דואר אלקטרוני שבה אתה מקבל דיוורי e-Med או זו שציינת בכרטיס האישי שלך.
קישור לאיפוס סיסמא נשלח למייל.
חזרה להתחברות
תגובות אחרונות