 מבוא
מבוא
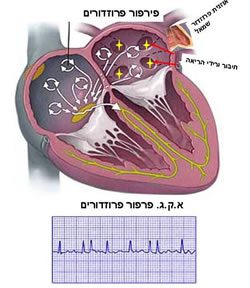
פרפור פרוזדורים (פ”פ) – Atrial Fibrillation – הפרעת קצב הלב השכיחה ביותר ממשיכה להטריד אותנו הרופאים למרות התקדמות הטיפול. שכיחותה של ההפרעה עולה בד בבד עם עלית גיל האוכלוסייה ובמקביל גורמת לעליה בתחלואה ובהוצאה הציבורית למערך הבריאות/המבטח.
קיימים דיווחים על עלייה של כ- 250% בשיעור האשפוזים עקב פרפור פרוזדורים בחולי (פ”פ) מעל גיל 65. על פי נתונים בינלאומיים, סובלים מההפרעה מדי שנה כ-7 מיליון אמריקאים [1]. בישראל סובלים מהתופעה כ-45 אלף ישראלים, והיא הגורם המרכזי לשבץ מוחי[2].
חשוב לזכור כי למרות שפ”פ מלווה מחלות של המסתם המיטרלי הגורמות להגדלת העליה השמאלית ועקב כך להפרעות הולכה תוך עלייתיות, היא שכיחה גם ללא פתלוגיה כלשהיא נילוות ונקראת lone AF .
קיימים מצבים נלווים המעלים שכיחות פ”פ כגון מחלת לב כלילית, יתר לחץ דם, סוכרת, הפרעות נשימה ושינה, משקל עודף, שתיית אלכוהול ופעילות יתר של בלוטת התריס. מצבים אלה אינם גורמים באופן ישיר להופעת פרפור אך קשורים לעליה בשכיחותו.
בכ 45% מהמקרים מופיעה פ”פ ללא מחלות נלוות באדם בריא באופן כללי.
פרפור פרוזדורים גורמת לאורך זמן להכפלת התמותה והתחלואה ממחלות לב וכלי דם והיא הסיבה השכיחה ביותר לאירוע מוחי תסחיפי[3].
הסכנות שבפרפור פרוזדורים:
הטיפול בפרפור פרוזדורים:
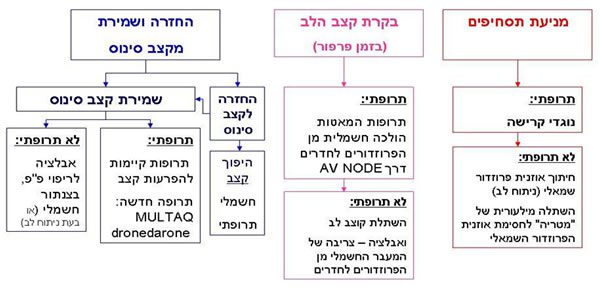
מטרת הטיפול הינה איזון הסימפטומים ומניעת תחלואה ותמותה. קיימות שלוש התייחסויות טיפוליות בפ”פ (תמונה 4):
א. מניעת היווצרות קרישי דם העלולים להישלח כתסחיפים למקומות שונים בגוף –
טיפול תרופתי: אנטיקואגולציה/ אנטיאגרגציה [4]
טיפול שאינו תרופתי: סגירת האוזנית של הפרוזדור השמאלי אשר הינה מקור היווצרות הקרישים והתסחיפים העיקרי בפרפור פרוזדורים במהלך ניתוח לב המבוצע מסיבה אחרת, כגון ניתוח החלפת מסתם, בצנתור [5] או בשיטה טורקוסקופית, זעיר פולשנית אם אינו מלווה פרוצדורה כירורגית אחרת[6]. סגירת האוזנית נחשבת לפרוצדורה פשוטה ובטוחה ומהווה פתרון מצויין לחולים שאינם יכולים לקבל טיפול בנוגדי קרישה.
ב. האטת קצב הלב בזמן הפרפור, עיקר סבלם של מרבית המתלוננים – ,Rate Control
טיפול תרופתי: כולל תרופות המאטות את ההולכה מן העליה לחדר דרך ה-A-V Node .
במטרה להגיע לדופק במנוחה מתחת ל-80 ובמאמץ לדופק של 110 עד 120 פעימות בדקה. לרוב משפרת האטת הדופק את הרגשתו של החולה[7].
טיפול שאינו תרופתי: כאשר לא ניתן להאט את קצב הלב באמצעים תרופתיים אפשר להשתיל קוצב לב ולבצע צריבה (אבלציה) בגלי רדיו של ה-A-V Node . הפעולה מבוצעת בצנתור ואינה מחייבת הרדמה כללית.
בתום הפעולה נוצרת חסימת הולכה מלאה בין הפרוזדור לעליה, והחולה תלוי לרוב בקצב הקוצב לב.
ניתן להשיג שליטה מוחלטת על מהירות קצב הלב ללא צורך בתרופות, אולם יש להמשיך בטיפול נוגד קרישה שכן פרפור הפרוזדורים עצמו לא נעלם. הפעולה מומלצת בחולים מבוגרים שלא ניתן לשלוט בקצב הלב או הנזקקים למגוון רב של תרופות כדי לשלוט בו.
ג. היפוך הפרפור והחזרת החולה לקצב סינוס ולשומרו במקצב זה – Rhythm Control [7].
החזרה לקצב סינוס: מוכרת במינוח היפוך קצב. ניתן להחזיר את החולה המפרפר לקצב סינוס ע”י מכת חשמל – Electrical Cardioversion או ע”י תרופות.
טיפולים שאינם תרופתיים לשמירת קצב סינוס:
צריבה באמצעות צנתר (אבלציה) בחולים עם אירועים חוזרים של פרפור וכישלון הטיפול התרופתי.
הטיפול ממושך ופולשני והוא מיועד לחולי פרפור התקפי שאינו קבוע, ללא מחלות רקע מורכבות.
שיעור הצלחת הפרוצדורה אינו גבוה ותלוי במיומנות הצוות המבצע[8,9].
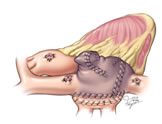
אין ספק כי הטיפול המושלם בפרפור פרוזדורים הינו ניתוח ה”מבוכים” המורכב maze ע”ש COX שפותח בתחילת שנות התשעים ושהציג כמעט 100% הצלחה ושימור ארוך טווח של קצב סינוס. הניתוח הגדול הכולל חיתוך מלא של הפרוזדורים בכמה מישורים שונים ותפירתם מחדש, אינו מתאים אלה במידה ומבוצע ניתוח לב פתוח אחר.
הצטלקות קו התפרים גורמת להפסקת ההולכה האברנטית ולחזרה לקצב סדיר[10-12].
(תמונה מס’ 5)
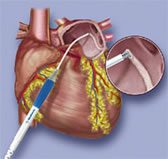
כיום החליפו שיטות צריבה מודרניות יותר את הצורך בחיתוך ותפירה של הפרוזדור. הצריבה בגלי רדיו, ליזר, קור ועוד אמורה ליצור תגובת הצטלקות הדומה לזו המתפתחת עקב ניתוח “המבוכים” המקורי של COX .
(תמונה מס’ 6)
שיעור הצלחת הצריבה בדרך הזו גבוה אך אינו מגיע לשיעור ההצלחה של הניתוח המקורי ונע בין 75%-85% בהתאם לסוג הפרפור (כרוני או התקפי) וסוגי האנרגיה השונים בהם משתמשים לצריבה[13,14] . המגבלה נובעת ככל הניראה מצריבה אוניפולרית החסרה בקרת איכות ועומק הצריבה (transmurality )[15].
הפתרון הכירורגי נשמר לחולים אשר שיטות הטיפול השמרניות יותר כשלו, לחולים סמפטומטיים או לכאלה שאינם יכולים/ רוצים ליטול נוגדי קרישה.
העדויות המדעיות המצטברות מעידות על שיפור משמעותי באיכות ותוחלת החיים בחולים שעברו אבלציה (צריבה) מוצלחת לעומת טיפול תרופתי[16].
“האור שבקצה המצלמה” – הטורקוסקופית
לאחרונה הוחל במרכז הרפואי “תל-אביב” עש סורסקי, שימוש בטורקוסקופיה לביצוע צריבה כירורגית על כל יתרונותיה. בשיטה זו מיושמת טכנולוגיה חדישה אותה ניתן להחדיר לתוך בית החזה דרך פתחים זעירים של מספר מילימטרים ולהעזר בטורקוסקופ (מצלמת וידאו בקוטר 5 ממ”). תמונה מס’ 7.
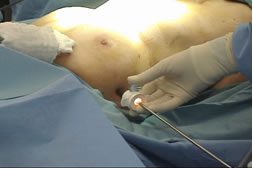
בהרדמה כללית יוצרים 2 פתחים בקוטר 12ממ” ופתח נוסף אחד בקוטר 5 ממ” בדופן בית החזה הימני. דרך הפתחים הזעירים ותחת הנחיית הטורקוסקופ מוחדר אל מתחת הלב מיכשור הצריבה העדין והחדיש – Gemini של חברת מדטרוניק המאפשר הקפה מלאה ובידוד הדופן האחורי של העליה השמאלית בדיוק רב וכפי שצפה COX בניתוחו המסורתי.
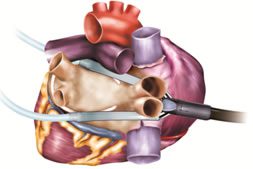
לאחר מכן מוחדר המכשיר בדיוק באןץן האופן דרך דופן בית החזה השמאלי להשלמת תמונת הראי של הצריבה ליצירת רצף הצריבה המתוכנן הקרוי box lesion [17]. ניתן להשתמש גם במיכשור חדיש נוסף הנקרא Cardioblate MAPS . באמצעותו מזהים מוקדים חשמליים עצמונים לא רצויים באיזור הגנגליונים הסימפטיים הניתנים לצריבה באופן מכוון ואף לאשר באמצעותו את הצלחתה [18].
את הפרוצדורה משלימים בכריתה אנדוסקופית של אוזנית הפרוזדור השמאלי המהווה מקור לכ- 95% מהקרישים התסחיפים המסוכנים[19].
בסיום התהליך הנמשך כשעתיים מושאר מכל צד של בית החזה נקז, המוצאים בבוקר למחרת. לאחר מספר שעות ניתן לשחרר את המטופל לביתו. קצב ההחלמה מהיר והחזרה לקצב סדיר הדרגתית ברוב המקרים.
יתרונו הבולט של המכשור החדיש מעבר לעובדת היותו מוחדר בשיטה טורקוסקופית מינימליסטית נעוץ בעובדת היותו מופעל בטכנולוגית bi-polar [15] . טכנולוגיה זו מדגימה באופן הדומה ביותר את הפיסיולוגיה הכירורגית של COX שכן היא מאפשרת הבטחת איכות ועומק הצריבה שאינה מתאפשרת בטכנולוגיות אחרות.
שיטה זו הצליחה יפה בחולים קשים ועמידים לטיפולים אחרים בכללם הלוקים בפרפור כרוני עיקש.
ההבנה של מנגנוני הפרעת הקצב, עדכון הגישה הכירורגית הזעירה והסיכוי לריפוי המחלה הינם האור שבקצה המנהרה.
References
1. Miyasaka Y, Barnes ME, Gersh BJ, et al. Secular trends in incidence of atrial fibrillation in Olmsted County, Minnesota, 1980 to 2000, and implications on the
projections for future prevalence. Circulation. 2006;114:119-25.
2. Kannel WB, Abbott RD, Savage DD, et al. Epidemiology features of chronic
atrial fibrillation: the Framingham Study. N Engl J Med. 1982;306:1018-22.
3. Hylek EM, DAntonio J, Evans-Molina C, et al. Translating the results of randomized trials into clinical practice. Stroke. 2006;37:1075-80.
4. Stroke Prevention in Atrial Fibrillation Investigators. Stroke Prevention in
Atrial Fibrillation Study: final results. Circulation. 1991;84:52739.
5. Holmes DR, Reddy VY, Turi ZG, et al. Percutaneous closure of the left
atrial appendage versus warfarin therapy for prevention of stroke in
patients with atrial fibrillation: a randomised non-inferiority trial. Lancet.
2009;374:53442.
6. Beyer E, Lee R, Lam BK. Minimally invasive bipolar radiofrequency ablation of lone atrial fibrillation: Early multicenter results
The Journal of Thoracic and Cardiovascular Surgery. 2009;137:3: 521-527.
7. Roy D, Talajic M, Nattel S, et al. Rhythm control versus rate control for
atrial fibrillation and heart failure. N Engl J Med. 2008;358:266777.
10. Connolly SJ, Pogue J, Hart RG, et al. Effect of clopidogrel added to
aspirin in patients with atrial fibrillation. N Engl J Med. 2009;360:
206678.
8. Calkins H, Reynolds MR, Spector P, et al. Treatment of atrial fibrillation
with antiarrhythmic drugs or radiofrequency ablation: two systematic
literature reviews and meta-analyses. Circ Arrhythm Electrophysiol.
2009;2:34961.
9. Cappato R, Calkins H, Chen SA, et al. Updated worldwide survey on the
methods, efficacy, and safety of catheter ablation for human atrial fibrillation.
Circ Arrhythm Electrophysiol. 2010;3:32 8.
10. Cox JL, Schuessler, DAgostino HJ Jr, et al. The surgical treatment of atrial fibrillation.
III. Development of a definitive surgical procedure. J Thorac Cardiovasc
Surg. 1991;101:569-83.
11. Cox JL, Ad N, Palazzo T, et al. Impact of the Maze procedure on the stroke rate in
patients with atrial fibrillation. J Thorac Cardiovasc Surg. 1999;118:833-40.
12. Stulak JM, Sundt TM, Dearani JA, et al. Ten-year experience with the Cox-Maze
procedure for atrial fibrillation: how do we define success? Ann Thorac Surg.
2007;83:1319-25.
13. McCarthy PM, Gillinov AM, Castle L, et al. The Cox-Maze procedure: the Cleveland Clinic experience. Semin Thorac Cardiovasc Surg. 2000;12:25-9.
14. Lee R, Takaski N, Schuessler RB, et al. The closed heart MAZE: a nonbypass surgical technique. Ann Thorac Surg. 1999;67:1692-702.
15. Gillinov AM, McCarthy PM, Blackstone EH, et al. Surgical ablation of atrial fibrillation with bipolar radiofrequency as the primary modality. J Thorac Cardiovasc
Surg. 2005;129:1322-9.
16. Prasad SM, Maniar HS, Camillo CJ, et al. The Cox maze III procedure for atrial fibrillation: long-term efficacy in patients undergoing lone versus concomitant procedures. J Thorac Cardiovasc Surg. 2003;126:1822-8.
17. Pruitt JC, Lazzara RR, Ebra G, et al. Minimally invasive surgical ablation of atrial
fibrillation: the thoracoscopic box lesion approach. J Interv Card Electrophysiol.
2007;20:83-7.
18. Lemola K, Chartier D, Yeh YH, et al. Pulmonary vein region ablation in the experimental vagal atrial fibrillation role of pulmonary veins versus autonomic ganglia. Circulation. 2008;117:470-7.
19. Blackshear JL, Odell JA. Appendage obliteration to reduce stroke in cardiac surgical patients with atrial fibrillation. Ann Thorac Surg. 1996;61:755-9.














השאירו תגובה
רוצה להצטרף לדיון?תרגישו חופשי לתרום!