הודעת טקדה
האישור הופך את אנטיביו לטיפול תחזוקתי היחיד שאושר בכל רחבי אירופה עם אופציות של הרכבים תת עוריים ותוך ורידיים לחולים מבוגרים עם קוליטיס כיבי או מחלת קרוהן.
שיטת טיפול נוספת המספקת לחולים באירופה יותר אפשרויות למתן טיפול ביולוגי סלקטיבי
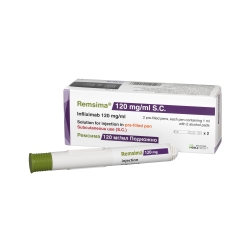
חברת התרופות טקדה הכריזה היום שהנציבות האירופית העניקה אישור לשווק את ההרכב התת העורי של אנטיביו (Vedolizumab) – תכשיר ביולוגי סלקטיבי למעי לשימוש כטיפול תחזוקתי אצל מבוגרים עם מחלה בינונית עד חמורה של קוליטיס כיבי או מחלת קרוהן. אנטיביו תת עורי יהיה זמין גם במזרק ממולא מראש וגם בעט-מזרק ממולא מראש.
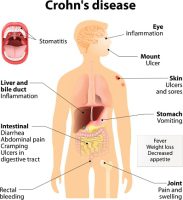
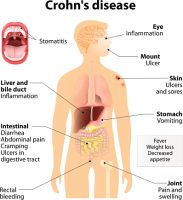
קוליטיס כיבי ומחלת קרוהן הינן שתי הצורות הנפוצות ביותר של מחלות מעיים דלקתיות והן פוגעות ביותר משני מיליון איש ברחבי אירופה.[1][2]. משמעות ההחלטה של הנציבות האירופית הינה שאנטיביו תת עורי מאושר כעת לשימוש ב27 מדינות החברות באיחוד האירופי, בנוסף לממלכה המאוחדת, נורווגיה, ליכטנשטיין ואיסלנד.
“אנחנו מאד שמחים שנציבות אירופית אישרה את ההרכב התת עורי של אנטיביו. זה מאפשר לרופאים ולחולים מבוגרים לבחור את צורת מתן הטיפול, אשר עובדת הכי טוב ומתאימה ביותר לכל מטופל באופן אישי” אומר אדם זסקה (Adam Zaeske), ראש היחידת ה-GI של אירופה וקנדה בטקדה. “משמעות מחוייבותה של טקדה לטפל במחלות גסטרואנטרולוגיות הינה שאיפתנו התמידית למצוא דרכים לחדש ולספק אפשרויות טיפול טובות יותר כדי לעמוד בצרכים של המטופלים שאנו משרתים”.
אישורה של הנציבות האירופית מתבסס על מחקר הציר 3VISIBLE , אשר העריך את הבטיחות והיעילות של ההרכב התת עורי של אנטיביו כטיפול תחזוקתי בחולים מבוגרים עם מחלה בינונית עד חמורה של קוליטיס כיבי או מחלת קרוהן, אשר השיגו תגובה* קלינית בשבוע 0 ו-2. [3][4][5] נתונים מניתוח ביניים של מחקר מתמשך, ארוך טווח, מורחב ופתוח VISIBLE 1 ו VISIBLE 2 גם כן נלקחו בחשבון. [6]
טקדה מאמינה מאד בתועלת שאנטיביו תת עורי יכול להביא לחולים מבוגרים, אשר חיים עם מחלה בינונית עד חמורה של קוליטיס כיבי או מחלת קרוהן, ונותרת מחויבת לעבודה עם רשויות רגולטוריות כדי להעניק את האופציה החשובה הזאת לחולים מהר ככל האפשר. בנוסף לקבלת האישור מנציבות אירופית, אנטיביו תת עורי הוגש לבחינה רגולטורית ברשויות רגולטוריות אחרות ברחבי העולם.
VISIBLE 1– קוליטיס כיבי: תגובה קלינית מוגדרת כירידה בציון המאיו Mayo score)) השלם של ≥3 נקודות ו≥30% מקו הבסיס (שבוע 0) עם ירידה נלווית בציון המשנה של דימום הרקטאלי ≥1 נקודות או תת נקודה כוללת של דימום רקטאלי של ≤1 נקודות. 4
VISIBLE 2– מחלת קרוהן: תגובה קלינית מוגדרת כירידה של ≥70 נקודות בציון אינדקס הפעילות של מחלת הקרוהן (CDAI) ממדד הבסיס (שבוע 0). [7]
[1] Jairath V, Feagan BG. Global burden of inflammatory bowel disease. Lancet Gastroenterol Hepatol. 2020;5:2-3.
[2] Baumgart DC, Carding SR. Inflammatory bowel disease: cause and immunobiology. Lancet. 2007;369:1627-1640
[3]Sandborn WJ, Baert F, Danese S, et al. Efficacy and safety of vedolizumab subcutaneous formulation in a randomized trial of patients with ulcerative colitis. Gastroenterology. 2020;158:562-572.
[4] יעילות ובטיחות של vedolizumab תת עורי כטיפול תחזוקתי בקוליטיס כיבי. זמין ב- https://clinicaltrials.gov/ct2/show/NCT02611830. . עודכן לאחרונה: 23 בינואר, 2020. גישה אחרונה: מאי 2020.
[5] יעילות ובטיחות של vedolizumab תת עורי כטיפול תחזוקתי במחלקת הקרוהן. זמין ב- https://clinicaltrials.gov/ct2/show/NCT02611817. . עודכן לאחרונה: 12 בנובמבר, 2019. גישה ארחונה: מאי 2020.
[6] מחקר הרחבה מתמשך עם תגית פתוחה לטווח ארוך על Vedolizumab תת עורי. זמין ב- https://clinicaltrials.gov/ct2/show/NCT02620046. עודכן לאחרונה: 12 בנובמבר, 2019. גישה אחרונה: מאי 2020.
[7] Vermeire S, Sandborn W, Baert F, et al. Efficacy and safety of vedolizumab SC in patients with moderately to severely active Crohns disease: Results of the VISIBLE 2 study. J Crohns Colitis. 2020;14:SO20-S021.













השאירו תגובה
רוצה להצטרף לדיון?תרגישו חופשי לתרום!