הודעת רדהיל
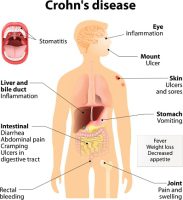
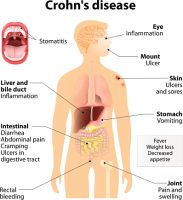
חברת הביו-פרמצבטיקה הישראלית, רדהיל ביופארמה , המתמקדת בתרופות אוראליות מסוג מולקולות קטנות, מוגנות פטנט, בשלבי פיתוח קליניים מתקדמים, לטיפול במחלות הקשורות לדרכי העיכול ובמחלות דלקתיות ובכלל זה סרטן, דיווחה היום כי לאחר ניתוח ביניים של נתוני בטיחות על-ידי ועדת נתונים ובטיחות בלתי-תלויה (DSMB) בניסוי שלב III עם RHB-104 למחלת הקרוהן, המליצה הועדה, פה אחד, להמשיך את הניסוי, ללא כל שינוי.
ניתוח שני של ועדת ה- DSMB צפוי ברבעון השני של 2017 ויכלול ניתוח ביניים של נתוני יעילות, כמו גם הערכה של האפשרות לעצירה מוקדמת של הניסוי במקרה של הצגת יעילות מובהקת, בכפוף לקריטריונים אשר נקבעו מראש.
הניסוי שלב III הראשון המתנהל כעת עם תרופת RHB-104 (ניסוי MAP US) הינו ניסוי אקראי, כפול-סמיות ומבוקר פלצבו, אשר נועד לבחון את הבטיחות והיעילות של RHB-104 כטיפול במחלת הקרוהן. 242 חולים גויסו לניסוי עד כה, מתוך סך כולל מתוכנן של 410 חולים ב-עד 150 מרכזים קליניים בארה”ב, קנדה, אירופה, ישראל, אוסטרליה וניו-זילנד.
אודות רדהיל
רדהיל ביופארמה הינה חברת פרמצבטיקה הממוקמת בישראל ומתמקדת בתרופות אוראליות, מסוג מולקולות קטנות, מוגנות פטנט בשלבי פיתוח קליניים מתקדמים לטיפול ומחלות הקשורות לדרכי העיכול ובמחלות דלקתיות ובכלל זה סרטן. צנרת התרופות מוגנות הפטנט של החברה כוללת: (i) RHB-105 – קומבינציה במתן אוראלי לטיפול בזיהום של חיידק ה- Helicobacter pylori – עם תוצאות חיוביות מניסוי שלב III ראשון; (ii)RHB-104 – קומבינציה במתן אוראלי לטיפול במחלת הקרוהן – ניסוי שלב III ראשון מתנהל כעת, ולטיפול בטרשת נפוצה – ניסוי שלב IIa הושלם; (iii) BEKINDA® (RHB-102) – תרופה במתן כדור חד-יומי אוראלי של חומר הפעיל ondansetron למניעת בחילות והקאות עם ניסוי שלב III המתנהל כעת לטיפול בגסטרואנטריטיס חריפה וגסטריטיס, וניסוי שלב II המתנהל כעת לטיפול בתסמונת המעי הרגיז; (iv) RHB-106 – כדור אוראלי לריקון המעי כהכנה לפרוצדורות רפואיות אשר נמכרה בהסכם רישיון כלל-עולמי ל- Salix Pharmaceuticals Ltd. (v) (ABC294640) YELIVA® – תרופה חדשנית, מעכבת SK2 במתן אוראלי, הנמצאת בשלב II ומיועדת לטיפול בסרטן, מחלות דלקתיות ומחלות בדרכי העיכול; (vi) MESUPRON – תרופה חדשנית, מעכבת uPA במתן אוראלי, המיועדת לטיפול בגידולים סרטניים של דרכי העיכול וגידולים סרטנים מוצקים נוספים – שני ניסויי שלב II הושלמו; (vii) RIZAPORT®(RHB-103) – דפית מסיסה אוראלית המכילה rizatriptan לטיפול במיגרנה, אשר בגינה הוגשה בקשה לאישור שיווק בארה”ב הנמצאת בבחינה של ה- FDA ונתקבל אישור שיווק בגרמניה באוקטובר ;2015 למידע נוסף: www.RedHillbio.com













השאירו תגובה
רוצה להצטרף לדיון?תרגישו חופשי לתרום!