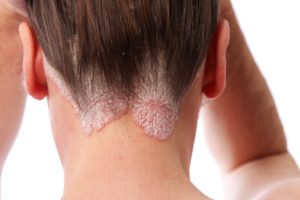
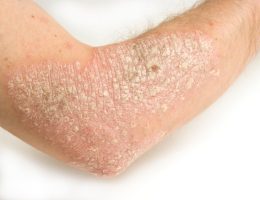
Bimekizumab יעיל ונסבל היטב, כך עולה ממחקר חדש מנתוני עולם-אמיתי, בדומה לתוצאות דומות שהודגמו במחקרים הקליניים של התרופה בפאזה 3 שהובילו לאישורה. Bimekizumab הוא נוגדן חד שבטי המכוון כנגד IL17A ו-IL17F , המאושר לטיפול בפלאק פסוריאזיס בדרגת חומרה בינונית עד קשה.
המחקר, שפורסם ב-Frontiers in Medicine , הינו המחקר המשמעותי הראשון אשר מדגים את היעילות של Bimekizumab בעולם האמיתי.
מחקר רטרוספקטיבי, רב-מרכזי זה כלל חולים הסובלים מפסוראיזיס רובדית בדרגת חומרה בינונית עד קשה שטופלו ב Bimekizumab ב-19 בתי חולים באיטליה בין 2022 ל-2023. המחקר כלל 237 חולים שקיבלו לפחות זריקה אחת של bimekizumab, מתוכם 171 חולים ו-114 חולים השלימו 4 ו-16 שבועות של מעקב, בהתאמה.
היעילות של bimekizumab הוערכה בשיעור השיפור במדד ה PASI בהשוואה לנקודת ההתחלה בשבועות 4 ו -16. התוצאות העיקריות היו אחוז החולים שהשיגו שיפור של לפחות 75% ,(PASI75) 90% (PASI90) ו- 100% (PASI100) בציון PASI. 43.3% ו-75.4% מהמטופלים השיגו עור נקי ((PASI100 בשבועות 4 ו-16, בהתאמה.
השיפור המהיר ב-PASI היה קשור גם לירידה בממוצע ה- DLQI לאורך תקופת המחקר, 60.2% ו- 86.8% דיווחו על DLQI של 0/1 לאחר 4 ו-16 שבועות, בהתאמה.
בנוסף, לא נצפו הבדלים מובהקים בין מטופלים ביו-נאיבים לאלו שטופל בטיפול ביולוגי בעבר במונחים של שיפור במדדי PASI75, PASI90 ו- PASI100. תופעת הלוואי השכיחה ביותר שדווחה במחקר היתה קנדידה אורלית (oral candidiasis) (10.1%), ולא נצפו תופעות לוואי חמורות או תופעות לוואי שהובילו להפסקת הטיפול במהלך המחקר.
לסיכום, בחינה של נתוני העולם האמיתי מאשרת את היעילות של bimekizumab, בטווח הקצר נצפו תגובות דומות או טובות יותר ביחס לניסויים קליניים. במחקר זה, חולים ביו-נאיביים הראו תגובות מעט טובות יותר בשבוע 4, אך לא היו הבדלים משמעותיים לאחר 16 שבועות בקרב חולים שכבר טופלו בתרופות ביולוגיות אחרות. לא נמצאו ממצאי בטיחות משמעותיים לאורך תקופת המחקר.
Front Med (Lausanne). 2023 Aug 8:10:1243843
המידע מוגש בחסות חברת ניאופרם (ישראל) 1996 בע”מ
לפרטים נוספים ולדיווח תופעות לוואי ניתן לפנות למחלקת הרפואה בניאופרם, טל’: 1-800-250-255, פקס: 03-9373716, בנין ניאופרם, השילוח 6, ת.ד 7063, פתח תקווה 4917001.
1912-NOV-2023










השאירו תגובה
רוצה להצטרף לדיון?תרגישו חופשי לתרום!