הודעת רוש
- נתוני יעילות אקספלורטוריים הראו כי לאחר שנתיים, 88% מהתינוקות שטופלו ב- Evrysdi היו בחיים ולא הזדקקו להנשמה קבועה
- 59% מהתינוקות היו מסוגלים לשבת ללא תמיכה למשך 5 שניות לפחות
- לא זוהו נתוני בטיחות חדשים
- בחודש אוגוסט ה-FDA אישר את התרופה Evrysdi לטיפול ב-SMA במבוגרים ובילדים בגילאי חודשיים ומעלה
חברת Roche) הכריזה על תוצאות חדשות מחלק 1 של מחקר הציר FIREFISH לאחר שנתיים של טיפול עם Evrysdi (Risdiplam) בתינוקות בגילאי חודשיים עד שבעה חודשים עם ניוון שרירים שדרתי (SMA) מסוג 1 סימפטומטיים. התוצאות לאחר שנתיים של טיפול בתינוקות אשר טופלו במינון התרפויטי של Evrysdi (17/21) הראו כי הם ממשיכים להשתפר ולהשיג אבני דרך מוטוריות.
ניתוח הנתונים האקספלורטורי הדגים כי לאחר שנתיים, כ-88% מהתינוקות היו בחיים ולא הזדקקו להנשמה קבועה. בנוסף לכך, לאחר שנתיים, 59% (10/17 לעומת 7/17 לאחר שנה) מהתינוקות היו מסוגלים לשבת ללא תמיכה למשך 5 שניות לפחות, כפי שהוערך באמצעות סולם המוטוריקה הגסה מתוך סולם ביילי להתפתחות תינוקות – מהדורה שלישיתBSID-III ). 65% (11/17 לעומת 9/17 לאחר שנה אחת) שמרו על היכולת להחזיק את הראש זקוף, 29% (5/17 לעומת 2/17 לאחר שנה אחת) היו מסוגלים להתהפך לבד ו-30% (5/17 לעומת 1/17 לאחר שנה אחת) היו מסוגלים לעמוד בצורה עצמאית או עם תמיכה. לאחר שנתיים של טיפול עם Evrysdi, 71% (12/17 לעומת 10/17 לאחר שנה אחת) מהתינוקות השיגו ציון CHOP-INTEND* של 40 נקודות או יותר, וכל התינוקות שיפרו את הציון בין חודש 12 לחודש 24. מבין התינוקות שהיו בחיים לאחר שנתיים (n=14), 100% שמרו על היכולת לבלוע ו-93% (13/14) הצליחו לאכול דרך הפה. הבטיחות עבור Evrysdi במחקר FIREFISH תאמה את פרופיל הבטיחות שדווח בעבר ולא זוהו נתוני בטיחות חדשים. תופעות הלוואי השכיחות ביותר (n=21) כללו חום (71%), זיהום בדרכי הנשימה העליונות (52%), שיעול (33%), הקאות (33%), שלשולים (29%) וזיהום בדרכי הנשימה (29%). תופעת הלוואי החמורה ביותר אשר אירעה ב-24% מהתינוקות הייתה דלקת ריאות.
“אנו מעודדים מאוד מהתוצאות המתקבלות בשנה השנייה של הטיפול ב-Evrysdi,” כך לדברי ד”ר לוי גאראווי, M.D., Ph.D., קצין הרפואה הראשי ומנהל פיתוח מוצר גלובלי בחברת Roche. “תוצאות אלה מוסיפות ליעילות ולבטיחות אשר הודגמו עבור Evrysdi במחקרי הציר, ואנו מצפים בכיליון עיניים להמשך ההערכה הן של ההישרדות והן של התפקוד המוטורי במעקב ארוך טווח לטיפול זה, שהינו הראשון מסוגו.”
בעת הניתוח, התינוק הצעיר ביותר היה בן 28.4 חודשים והבוגר ביותר היה בן 45.1 חודשים. הגיל החציוני בעת הגיוס היה 6.3 חודשים. מבין 17 התינוקות שטופלו במינון התרפויטי, שניים חוו סיבוכים קטלניים של מחלתם לאחר 8 ו-13 חודשי טיפול, ותינוק אחד הוצא מהמחקר ולמרבה הצער נפטר כעבור 3.5 חודשים. אף אחד מהמקרים האלו לא יוחס על ידי החוקר כקשור ל-Evrysdi.
הנתונים הוצגו בכנס השנתי הבין לאומי ה-25 הווירטואלי של אגודת World Muscle Society.
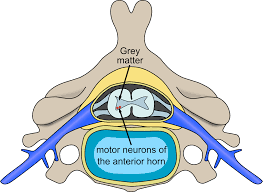
Evrysdi נחקרת בקרב למעלה מ-450 חולים כחלק מתוכנית ניסויים קליניים גדולה ומבוססת היטב בנושא SMA. התוכנית כוללת משתתפים מגיל לידה ועד מבוגרים בני 60, לרבות חולים אשר עדיין לא פיתחו תסמינים וחולים אשר טופלו בעבר בטיפולים ממוקדים אחרים למחלת SMA. Evrysdi מיועדת לטיפול ב-SMA על ידי הגברת ייצור החלבון survival of motor neuron (SMN) ושמירה על רמות הייצור המוגברות. חלבון ה-SMN מצוי בכל חלקי הגוף והינו חיוני לשמירה על נוירונים מוטוריים בריאים ולשמירה על יכולת התנועה. חברתRoche מובילה את הפיתוח הקליני שלEvrysdi כחלק משיתוף פעולה עם קרן SMA Foundation ועם חברת PTC Therapeutics.
*CHOP-INTEND – Childrens Hospital of Philadelphia Infant Test of Neuromuscular Disorders
* בדיקה לתינוקות לגילוי הפרעות עצב-שריר, בית החולים לילדים של פילדלפיה
אודות Evrysdi (Risdiplam)
Evrysdi היא משנה שחבור ניסיוני של survival of motor neuron 2 (SMN2), המיועד לטיפול ב- SMA, הנגרם בשל מוטציות בכרומוזום 5q אשר מובילות לחסר בחלבון SMN. Evrysdi, תרופה נוזלית, ניתנת בבית מדי יום, במתן פומי או דרך צינור הזנה.
ה-FDA אישר את השימוש ב-Evrysdi לטיפול ב-SMA במבוגרים ובילדים בגילאי חודשיים ומעלה.
Risdiplam קיבלה מעמד PRIME על ידי רשות הסוכנות התרופות האירופאית (EMA) בשנת 2018 ומעמד של תרופת יתום על ידי ה-FDA וה-EMA בשנת 2017 ו- 2019, בהתאמה. נכון להיום, הוגשו בקשות עבורEvrysdi ב-16 שווקים בינלאומיים: אוסטרליה, ברזיל, צ’ילה, הודו, אינדונזיה, ישראל, כווית, מקדוניה, מלזיה, רוסיה, סינגפור, דרום קוריאה, טייוואן, תאילנד, אוקראינה ואיחוד האמירויות הערביות. בנוסף לכך, ארבע רשויות בריאות ברחבי העולם בודקות בימים אלה את הבקשה: קנדה, סין, האיחוד האירופי ושוויץ.
Risdiplam עוברת כיום הערכה בארבעה ניסויים רב-מרכזיים באנשים עם SMA:
- (FIREFISH)NCT02913482 מחקר ציר קליני, בתוית פתוחה ‘ בן שני חלקים בתינוקות עם SMA סוג 1. חלק 1 היה מחקר במינון עולה בקרב 21 תינוקות, אשר מטרתו העיקרית הייתה להעריך את פרופיל הבטיחות של Risdiplam בתינוקות ולקבוע את המינון עבור חלק 2. חלק 2 הוא מחקר MHR חד-זרועי להערכת Risdiplam בקרב 41 תינוקות עם SMA סוג 1 אשר טופלו למשך שנתיים, ולאחריו מחקר המשך בתווית פתוחה. הגיוס לחלק 2 הושלם בנובמבר 2018. המטרה העיקרית של חלק 2 הייתה להעריך את היעילות כפי שנמדדה על פי אחוז התינוקות שהיו מסוגלים לשבת ללא תמיכה לאחר 12 חודשי טיפול, כפי שהוערך באמצעות סולם המוטוריקה הגסה מתוך מבחן ביילי להתפתחות תינוקות – מהדורה שלישית (BSID-III) (מוגדר כישיבה ללא תמיכה למשך 5 שניות). המחקר השיג את מדד ההערכה העיקרי שלו.
- SUNFISH – )NCT02908685( הינו מחקר ציר, כפול סמיות, מבוקר פלצבו בן שני חלקים הנערך באנשים בני 25-2 שנים עם SMA סוג 2 או 3. חלק 1 (n=51) קבע את המינון לחלק 2 המאשש. חלק 2 (n=180) העריך את התפקוד המוטורי תוך שימוש בניקוד כולל על פי מדד Motor Function Measure 32 (MFM-32) לאחר 12 חודשים. MFM-32 הינו סולם מאומת המשמש להערכת תפקוד מוטורי עדין וגס בקרב הסובלים מהפרעות נוירולוגיות, לרבות SMA. המחקר השיג את מדד ההערכה העיקרי שלו.
- JEWELFISH )NCT03032172) מחקר אקספלורטורי בתווית פתוחה המיועד לבחינת הבטיחות, הסבילות, הפרמקוקינטיקה (PK) והפרמקודינמיקה (PD) בחולי SMA בני 6 חודשים עד 60 שנים אשר טופלו בעבר בטיפולים ניסיוניים או מאושרים למחלת SMA למשך 90 ימים לפחות לפני קבלת Evrysdi. שלב הגיוס למחקר הסתיים (n=174).
- RAINBOWFISH )NCT03779334) מחקר בתווית פתוחה, חד-זרועי, רב-מרכזי, החוקר את היעילות, הבטיחות, הפרמקוקינטיקה והפרמקודינמיקה של Risdiplam בתינוקות (~n=25), מלידה ועד גיל שישה שבועות (בעת המנה הראשונה) עם אבחנה גנטית של SMA ושאינם מציגים עדיין תסמינים. המחקר נמצא בשלב גיוס משתתפים.
אודות SMA
ניוון שרירים שדרתי (SMA) היא מחלת עצב-שריר חמורה ופרוגרסיבית אשר עלולה להיות קטלנית. מחלה זו, המשפיעה על כ-1 מתוך כל 10,000 תינוקות, היא הסיבה הגנטית הנפוצה ביותר לתמותת תינוקות. SMA נגרמת כתוצאה ממוטציה בגן Survival Motor Neuron-1 (SMN1) שגורמת לחסר בחלבון SMN. חלבון זה מצוי בכל חלקי הגוף והוא חיוני לתפקוד העצבים ששולטים על השרירים ועל התנועה. ללא החלבון, תאי עצב אינם מסוגלים לתפקד כראוי, דבר המוביל להתפתחות חולשת שרירים לאורך זמן. כתלות בסוג ה-SMA, הכוח הפיזי של האדם הלוקה במחלה והיכולת שלו ללכת, לאכול או לנשום עלולים לפחות באופן משמעותי או להיאבד לחלוטין.














השאירו תגובה
רוצה להצטרף לדיון?תרגישו חופשי לתרום!